โพสต์ที่เกี่ยวข้อง
MS เชื่อมขวางสําหรับโปรตีนเชิงซ้อนสอนอะไรเกี่ยวกับการเปลี่ยนแปลงโครงสร้าง
2026-02-22Cross-Linking MS สําหรับโปรตีนคอมเพล็กซ์เป็นหนึ่งในวิธีที่ใช้งานได้จริงที่สุดในการ "แช่แข็ง" หน้าสัมผัสโปรตีนจริงให้เข้าที่แล้วอ่านออกด้วยแมสสเปกโตรเมตรี ดังนั้นคุณจึงสามารถเรียนรู้ว่าคอมเพล็กซ์เปลี่ยนรูปร่างอย่างไร ไม่ใช่แค่ลักษณะในสแน็ปช็อตเดียว ที่ Longlight Technology เราเห็นหลายทีมเริ่มต้นด้วยคําถามง่ายๆ: โปรตีนเชิงซ้อนของฉันคงที่หรือสลับไปมาระหว่างโครงสร้างที่สําคัญต่อการทํางาน บทความนี้จะอธิบายในวิธีที่เป็นมิตรกับผู้เริ่มต้นว่าการเชื่อมขวางทางเคมีควบคู่ไปกับแมสสเปกโตรเมตรี (มักเรียกว่า CL-MS หรือ XL-MS) สามารถสอนคุณเกี่ยวกับการเปลี่ยนแปลงโครงสร้างและวิธีเปลี่ยนผลลัพธ์ให้เป็นการตัดสินใจที่คุณสามารถดําเนินการได้
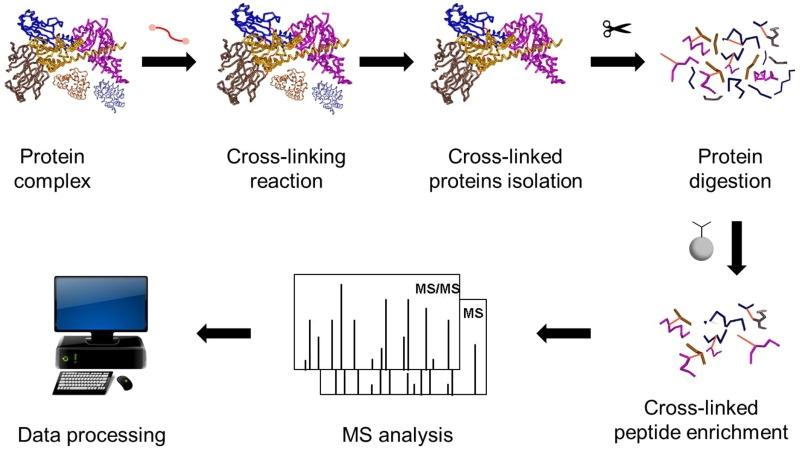
ความก้าวหน้าในการวิเคราะห์โปรตีนเชิงซ้อนโดยการเชื่อมขวางทางเคมีควบคู่ไปกับแมสสเปกโตรเมตรี
1) Cross-Linking MS คืออะไร?
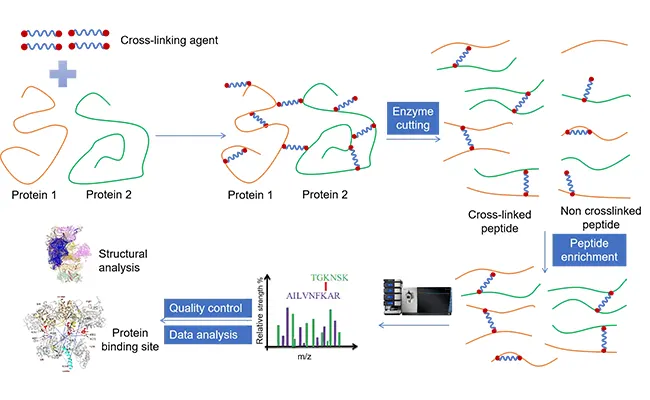
Cross-Linking MS (มักเขียนว่า XL-MS หรือ CL-MS) เป็นวิธีการที่ช่วยให้คุณค้นหาว่าส่วนใดของโปรตีนอยู่ใกล้กัน ไม่ว่าจะเป็นภายในโปรตีนหนึ่งหรือระหว่างโปรตีนในเชิงซ้อน โดยการ "เชื่อมโยง" ทางเคมีแล้วระบุการเชื่อมโยงเหล่านั้นด้วยแมสสเปกโตรเมตรี
นี่คือแนวคิดในภาษาอังกฤษธรรมดา:
• เพิ่มตัวเชื่อมขวาง ("สะพาน" เคมีขนาดเล็ก)
มันทําปฏิกิริยากับกรดอะมิโนจําเพาะและสามารถเชื่อมต่อสารตกค้างสองชนิดที่อยู่ในระยะที่จํากัดจากกันได้
• ย่อยโปรตีนเป็นเปปไทด์
เอนไซม์ (มักเป็นทริปซิน) ตัดโปรตีนออกเป็นชิ้นเล็กๆ
•เรียกใช้แมสสเปกโตรเมตรี
MS ตรวจจับเปปไทด์ รวมถึงคู่เปปไทด์ที่เชื่อมขวาง
•วิเคราะห์การเชื่อมโยงข้าม
การเชื่อมโยงข้ามที่ระบุแต่ละรายการจะกลายเป็นข้อจํากัดด้านระยะทาง:
"สารตกค้าง A และสารตกค้าง B อยู่ใกล้พอที่จะเชื่อมโยงกันภายใต้เงื่อนไขเหล่านี้"
ใช้ทําอะไร
• การทําแผนที่ปฏิสัมพันธ์ระหว่างโปรตีนกับโปรตีน (PPI): ใครสัมผัสใครในคอมเพล็กซ์
•การระบุอินเทอร์เฟซ: ภูมิภาคใดที่สร้างพื้นผิวสัมผัส
•การเปลี่ยนแปลงโครงสร้าง: เปรียบเทียบเงื่อนไข (apo vs ligand-bound, mutant vs WT) เพื่อดูผู้ติดต่อปรากฏ / หายไป
•รองรับการสร้างแบบจําลองโครงสร้าง: รวมกับ cryo-EM / X-ray เพื่อตรวจสอบหรือปรับแต่งแบบจําลอง
เหตุใดจึงมีค่า
•สามารถจับปฏิสัมพันธ์ที่อ่อนแอหรือมีอายุสั้น (ลิงค์โควาเลนต์ "ตรึง" พวกเขา)
• บ่อยครั้งที่ไม่จําเป็นต้องติดฉลากพิเศษ
•สามารถมีปริมาณงานค่อนข้างสูงสําหรับการเปรียบเทียบหลายเงื่อนไข
2) เหตุใดการเปลี่ยนแปลงโครงสร้างจึงยากมาก To จับภาพ
โปรตีนเชิงซ้อนจํานวนมากไม่นั่งนิ่ง พวกมันหายใจ หมุน เปิด ปิด และจัดเรียงหน่วยย่อยใหม่เพื่อตอบสนองต่อลิแกนด์ เกลือ pH ฟอสโฟริเลชัน หรือคู่จับ วิธีการโครงสร้างแบบดั้งเดิมอาจยอดเยี่ยม แต่มักจะชอบสถานะที่มั่นคง หากคอมเพล็กซ์มีความยืดหยุ่นประกอบอย่างอ่อนแอหรือมีอายุสั้นคุณอาจเห็นเพียงบางส่วนของเรื่องราว
การเชื่อมขวางช่วยได้เพราะสามารถเชื่อมต่อสารตกค้างสองชิ้นที่อยู่ในระยะทางที่กําหนดได้ ในภาษาธรรมดา มันทําเครื่องหมายว่า "ทั้งสองตําแหน่งนี้อยู่ใกล้พอที่จะสัมผัสได้" ณ เวลาที่เกิดปฏิกิริยา การเปรียบเทียบการเชื่อมโยงแบบเคียงข้างกัน - ปราศจากลิแกนด์กับที่ถูกผูกมัด เกลือต่ํา vs เกลือสูง ประเภทป่า vs กลายพันธุ์ - บอกคุณว่าคอมมิชชั่น ขยาย หรือกําหนดค่าใหม่ที่ซับซ้อน
✅ ข้อมูลเชิงลึกเชิงปฏิบัติสําหรับผู้เริ่มต้น: การเปลี่ยนแปลงโครงสร้างคือการเปลี่ยนแปลงของวงดนตรี XL-MS มองเห็นนอกเหนือจากโครงสร้างที่เสถียรที่สุดกับสเปกตรัมของสถานะในสารละลาย
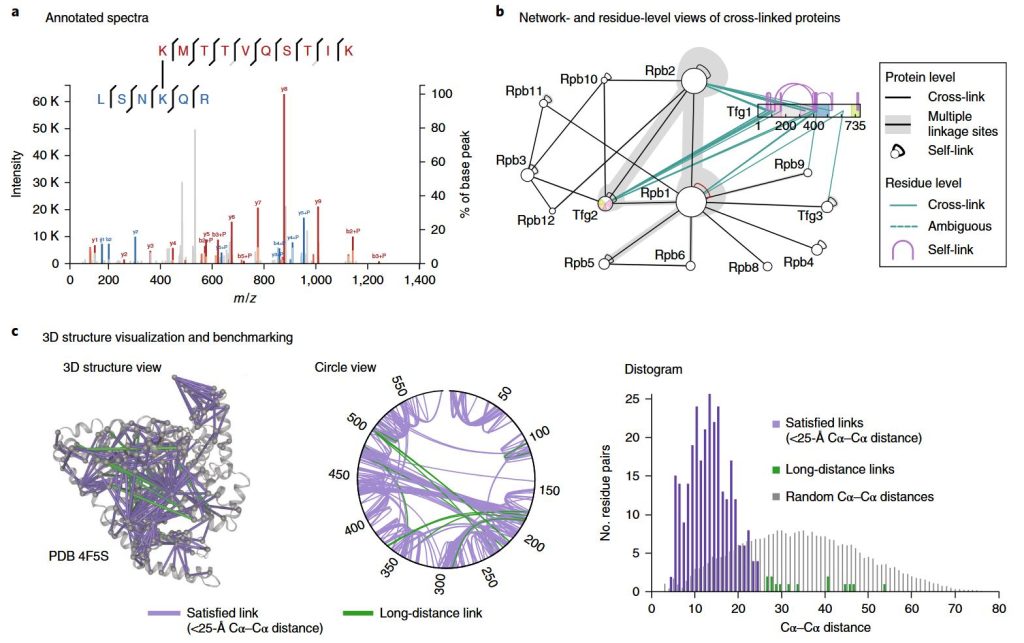
บริการเชื่อมขวางแมสสเปกโตรเมตรี | เอ็มโตซี ไบโอแล็บส์
การวัด MS แบบเชื่อมขวางในทางปฏิบัติคืออะไร
การเชื่อมขวางทางเคมีกับ MS จะวัดปริมาณความใกล้ชิดของสารตกค้างและรูปแบบปฏิสัมพันธ์ ซึ่งเป็นแนวทางมาตรฐานสําหรับการศึกษา PPI สารเชื่อมขวางทําปฏิกิริยากับกลุ่มฟังก์ชันบนโปรตีนและสามารถเชื่อมต่อโปรตีนที่มีปฏิสัมพันธ์ตั้งแต่สองตัวขึ้นไป (หรือสองตําแหน่งภายในโปรตีนเดียว) หลังจากการเชื่อมขวางแมสสเปกโตรเมตรีจะวิเคราะห์เปปไทด์ที่เชื่อมขวางช่วยให้คุณสามารถแสดงเครือข่ายปฏิสัมพันธ์และระบุสถานที่ดําเนินการได้
นั่นหมายความว่าอย่างไรสําหรับการเปลี่ยนแปลงโครงสร้าง?
•หากชุดของลิงก์ข้ามปรากฏขึ้นหลังจากการผูกลิแกนด์เท่านั้นจะแนะนําผู้ติดต่อใหม่ที่เกิดขึ้นในสถานะที่ถูกผูกไว้
• หากลิงก์ข้ามบางอย่างหายไป แสดงว่าไซต์เหล่านั้นไม่ได้ปิดอีกต่อไป อาจเป็นการเปิดคอมเพล็กซ์หรือย้ายโดเมน
• หากการเชื่อมโยงข้ามเปลี่ยนระหว่างยูนิตย่อย อาจบ่งบอกถึงการจัดเรียงยูนิตย่อยใหม่หรือเส้นทางการประกอบที่แตกต่างกัน
✅ สิ่งที่คุณได้รับจากวิธีนี้ (และเหตุใดจึงสําคัญ):
•ไม่จําเป็นต้องติดฉลากสารเคมีพิเศษ→คุณสามารถรักษาโปรตีนของคุณให้ใกล้เคียงกับรูปแบบดั้งเดิมและลดค่าใช้จ่ายในการทดลอง
•จับปฏิสัมพันธ์ที่มีอายุสั้น / อ่อนแอ→พันธะโควาเลนต์สามารถรักษาหน้าสัมผัสที่แตกสลายระหว่างการทําให้บริสุทธิ์หรือการวิเคราะห์
•ปริมาณงานสูงและความเร็วในการวิเคราะห์ที่รวดเร็ว→มีประโยชน์เมื่อคุณต้องการเปรียบเทียบเงื่อนไขหรือโครงสร้างจํานวนมากอย่างมีประสิทธิภาพ
•การเชื่อมขวางภายในเซลล์เป็นไปได้→สําหรับบางโครงการซึ่งจะช่วยให้คุณศึกษาคอมเพล็กซ์ที่ใกล้ชิดกับบริบทของเซลล์ดั้งเดิมมากกว่าในหลอดทดลองเท่านั้น
4) การอ่าน "การเคลื่อนไหว" จากรูปแบบ Cross-Link
ผู้เริ่มต้นบางครั้งคาดหวังว่าการเชื่อมโยงข้ามหนึ่งครั้งเท่ากับคําตอบเดียว ในทางปฏิบัติคุณค่ามาจากรูปแบบ
วิธีคิดที่เป็นประโยชน์คือ: การเชื่อมโยงข้ามเป็นข้อจํากัดด้านระยะทาง เมื่อคอมเพล็กซ์เปลี่ยนรูปร่างระยะห่างระหว่างสารตกค้างสองชิ้นจะเปลี่ยนไป XL-MS ไม่สามารถบอกมุมการหมุนที่แน่นอนได้เสมอไป แต่สามารถบอกคุณได้ว่าพื้นที่มีแนวโน้มที่จะเคลื่อนเข้าใกล้หรือห่างกันมากขึ้น และแผนที่ปฏิสัมพันธ์เปลี่ยนไปหรือไม่
นี่คือเรื่องราวโครงสร้างทั่วไปที่ XL-MS สามารถเปิดเผยได้:
✅ การบดอัด vs การเปิด
หากคุณเห็นการเชื่อมโยงข้ามภายในโปรตีนมากขึ้นซึ่งครอบคลุมพื้นที่ห่างไกลภายใต้เงื่อนไขเดียวโปรตีนอาจใช้สถานะที่กะทัดรัดมากขึ้น หากลิงก์เหล่านั้นหลุดในขณะที่ลิงก์อื่นๆ เพิ่มขึ้น มันอาจจะเปิดขึ้น
✅ การสลับอินเทอร์เฟซ
หากการเชื่อมโยงระหว่างยูนิตย่อย A และ B อ่อนตัวลง ในขณะที่การเชื่อมโยงระหว่าง A และ C แข็งแกร่งขึ้น แสดงว่ามีการถ่วงน้ําหนักใหม่หรือสวิตช์อินเทอร์เฟซ
✅ การรักษาเสถียรภาพโดยลิแกนด์หรือการกลายพันธุ์
ลิแกนด์ที่ "ล็อค" โครงสร้างมักจะเพิ่มความสามารถในการทําซ้ําของชุดการเชื่อมโยงข้ามที่เฉพาะเจาะจงและลดรูปแบบผสม
จากมุมมองในทางปฏิบัติสิ่งนี้สามารถแนะนําขั้นตอนต่อไปได้: การกลายพันธุ์ที่จะสร้างโดเมนใดที่จะตัดทอนเงื่อนไขบัฟเฟอร์ใดที่ทําให้คอมเพล็กซ์มีเสถียรภาพหรืออินเทอร์เฟซใดที่จะตรวจสอบด้วยวิธีอื่น
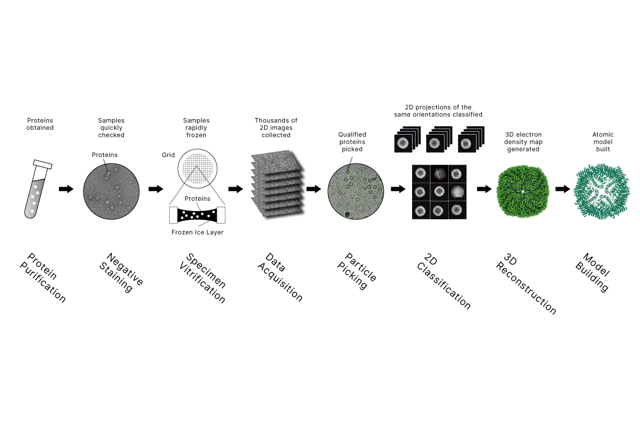
5) ผลลัพธ์ที่แข็งแกร่งขึ้นเมื่อใช้ XL-MS ร่วมกับ Cryo-EM หรือ X-Ray
XL-MS มักใช้ควบคู่ไปกับกล้องจุลทรรศน์อิเล็กตรอนแบบไครโอ (cryo-EM) และการเลี้ยวเบนของผลึกเอ็กซ์เรย์สําหรับการวิจัยโครงสร้างทางชีวภาพ การผสมผสานนี้มีประโยชน์อย่างยิ่งเมื่อการเปลี่ยนแปลงโครงสร้างเป็นคําถามหลัก
• Cryo-EM สามารถให้แบบจําลองโครงสร้างสําหรับสถานะที่โดดเด่น
• XL-MS สามารถตรวจสอบว่าโมเดลสอดคล้องกับพฤติกรรมของโซลูชันหรือไม่ และสามารถตั้งค่าสถานะทางเลือกที่ cryo-EM อาจสุ่มตัวอย่างน้อยเกินไป
• เอ็กซ์เรย์สามารถส่งโดเมนที่มีความละเอียดสูงในขณะที่ XL-MS ช่วยวางโดเมนภายในแอสเซมบลีที่ยืดหยุ่น
✅ เวิร์กโฟลว์ที่ใช้งานได้จริง: ใช้ XL-MS ก่อนเพื่อเรียนรู้ว่าคอมเพล็กซ์ของคุณแตกต่างกันหรือไม่ หากเป็นเช่นนั้น คุณสามารถออกแบบเงื่อนไขที่เสริมสร้างสถานะหนึ่งก่อนที่จะลงทุนอย่างมากในงานโครงสร้างที่มีความละเอียดสูง
6) เวิร์กโฟลว์การบริการ At เทคโนโลยี Longlight
ห้องปฏิบัติการหลายแห่งต้องการข้อมูลเชิงลึกของ Cross-Linking MS สําหรับโปรตีนคอมเพล็กซ์โดยไม่ต้องสร้างไปป์ไลน์เต็มรูปแบบภายในองค์กร เทคโนโลยี Longlight รองรับทั้งทีมที่มีประสบการณ์และผู้ใช้ครั้งแรกด้วยกระบวนการบริการที่ชัดเจน
คุณสามารถส่งตัวอย่างแบบเชื่อมขวาง หรือติดต่อเราเพื่อพัฒนาแผนการเชื่อมขวางแล้วส่งตัวอย่าง เราดําเนินการขั้นตอนการทํางานทั้งหมดให้เสร็จสมบูรณ์ รวมถึงการย่อยเอนไซม์ การเพิ่มคุณค่าเปปไทด์ การตรวจจับแมสสเปกโตรเมตรี การวิเคราะห์ข้อมูล และการส่งมอบรายงานการทดลอง แนวทางแบบ end-to-end นี้มีความสําคัญเนื่องจากการตีความตามโครงสร้างขึ้นอยู่กับการจัดการที่สอดคล้องกันในทุกขั้นตอน
✅ สิ่งนี้มีความหมายต่อคุณในฐานะลูกค้า:
•ข้อผิดพลาดในการส่งต่อระหว่างขั้นตอนน้อยลงและ "ไม่ทราบ" น้อยลงเมื่อคุณเปรียบเทียบเงื่อนไข
•รายงานที่จัดระเบียบเกี่ยวกับการตีความที่นําไปใช้ได้จริงไม่ใช่แค่การระบุดิบเท่านั้น
•ทําซ้ําได้เร็วขึ้นเมื่อคุณต้องการทดสอบโครงสร้างหรือเงื่อนไขการรักษาหลายอย่าง
หากโครงการที่กว้างขึ้นของคุณรวมถึงจีโนมิกส์หรือการพัฒนาการทดสอบต้นน้ํา Longlight ยังมีโซลูชันจีโนมที่ล้ําสมัย เครื่องมือในห้องปฏิบัติการขั้นสูง และรีเอเจนต์และวัสดุสิ้นเปลืองคุณภาพสูงที่ออกแบบมาเพื่อปรับปรุงประสิทธิภาพและความแม่นยําในห้องปฏิบัติการสมัยใหม่ ซึ่งสนับสนุนเวิร์กโฟลว์การวิจัยตั้งแต่ชีววิทยาโมเลกุลไปจนถึงการวิเคราะห์ที่แม่นยํา
7) CTA เชิงปฏิบัติ: เปลี่ยนคําถามเชิงโครงสร้างให้เป็นหลักฐานที่ทดสอบได้
การเปลี่ยนแปลงโครงสร้างไม่ใช่รายละเอียดด้านข้าง มันมักจะตัดสินว่าเป้าหมายนั้นใช้ยาได้หรือไม่คอมเพล็กซ์ประกอบอย่างถูกต้องหรือไม่และการกลายพันธุ์นั้นก่อกวนอย่างแท้จริงหรือไม่ MS แบบเชื่อมขวางสําหรับโปรตีนคอมเพล็กซ์ให้หลักฐานที่คุณสามารถเปรียบเทียบได้ตามเงื่อนไขต่างๆ ซึ่งช่วยให้คุณหยุดคาดเดาและเริ่มออกแบบ
✅ หากคุณกําลังวางแผนการศึกษาการเปลี่ยนแปลงโครงสร้าง ให้พิจารณาเริ่มต้นด้วย "ชุดเปรียบเทียบ" หนึ่งชุด:
• Apo vs ผูกลิแกนด์ (หรือผูกกับสารยับยั้ง)
• Wild-type เทียบกับการกลายพันธุ์ของอินเทอร์เฟซเดียว
• บัฟเฟอร์เสถียรหนึ่งตัวเทียบกับบัฟเฟอร์ความเครียดหนึ่งตัว (ช่วงเกลือ/pH)
ซีทีเอ: หากคุณต้องการแผน XL-MS ที่ชัดเจนและเป็นมิตรกับผู้เริ่มต้นซึ่งปรับให้เหมาะกับโปรตีนเชิงซ้อนของคุณ โปรดติดต่อ Longlight Technology เพื่อหารือเกี่ยวกับเป้าหมายของคุณ (การทําแผนที่ปฏิสัมพันธ์ การตรวจสอบอินเทอร์เฟซ หรือการเปรียบเทียบโครงสร้าง) เราสามารถช่วยคุณเลือกกลยุทธ์การเชื่อมโยงข้ามที่ใช้งานได้จริงและส่งรายงานที่ตีความได้ซึ่งสนับสนุนการทดลองครั้งต่อไปของคุณหรือแบบจําลองโครงสร้างถัดไปของคุณ