โพสต์ที่เกี่ยวข้อง
ChIP: เผยให้เห็นว่าโปรตีนควบคุมยีนอย่างไร: เริ่มต้นด้วยคําถามง่ายๆ ข้อเดียว
2026-02-25ChIP: การเปิดเผยว่าโปรตีนควบคุมยีนอย่างไรเป็นวิธีการปฏิบัติที่นักวิทยาศาสตร์ใช้เพื่อตอบคําถามที่เป็นศูนย์กลางของชีววิทยาสมัยใหม่: โปรตีนชนิดใดอยู่ในบริเวณ DNA ใดในเซลล์จริงภายใต้สภาวะจริง หากคุณยังใหม่กับการควบคุมยีน การคิดว่า DNA เป็นห้องสมุดและโปรตีนควบคุมเป็น "ผู้อ่าน" ที่เปิดหน้าเฉพาะในเวลาที่กําหนด ChIP (Chromatin Immunoprecipitation) คือวิธีที่เราจับภาพช่วงเวลานั้นและระบุหน้าเว็บ
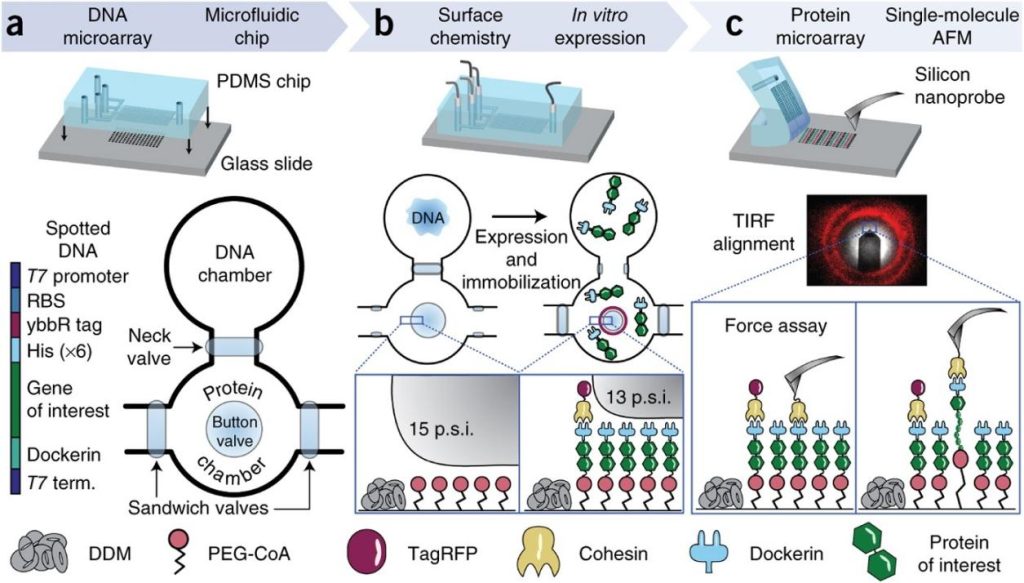
จากยีนสู่กลไกโปรตีนบนชิป วิธีการทางธรรมชาติ
ที่ Longlight Technology เราผลิตและสนับสนุนเครื่องมือเวิร์กโฟลว์หลักที่ใช้ในการวิจัยโครมาติน ตั้งแต่สิ่งจําเป็นในการจัดการตัวอย่างไปจนถึงตัวเลือกการเพิ่มคุณค่าและการตรวจจับดาวน์สตรีม เพื่อให้ทีมใหม่สามารถเริ่มต้นด้วยเส้นทางที่สะอาดและทําซ้ําได้ และทีมที่มีประสบการณ์สามารถปรับขนาดได้อย่างมั่นใจ
ChIP วัดอะไรได้บ้างและเหตุใดจึงสําคัญ
พูดง่ายๆ ก็คือ ชิป ทดสอบว่าโปรตีนมีความเกี่ยวข้องทางกายภาพกับบริเวณ DNA เฉพาะภายในเซลล์หรือไม่ มีการใช้กันอย่างแพร่หลายสําหรับปัจจัยการถอดความ ปัจจัยร่วม และการดัดแปลงฮิสโตน เนื่องจากสิ่งเหล่านี้เป็น "สวิตช์" ที่ตัดสินว่ายีนทํางาน หยุดชั่วคราว หรือเงียบ เวิร์กโฟลว์ ChIP มาตรฐานมักจะรวมถึงการเชื่อมขวาง (สําหรับหลายเป้าหมาย) การกระจายตัวของโครมาติน การเพิ่มคุณค่าด้วยแอนติบอดี การทําให้บริสุทธิ์ DNA และการอ่านข้อมูลโดย qPCR (กําหนดเป้าหมาย) หรือการจัดลําดับ (ทั่วทั้งจีโนม)
นี่คือเหตุผลที่ ChIP: การเปิดเผยว่าโปรตีนควบคุมยีนอย่างไรเป็นมากกว่าเทคนิคในห้องปฏิบัติการ แต่เป็นเครื่องมือในการตัดสินใจ ช่วยให้นักวิจัย:
✓ ยืนยันว่าตัวควบคุมที่น่าสงสัยผูกมัดโปรโมเตอร์หรือตัวเพิ่มประสิทธิภาพหรือไม่
✓ เปรียบเทียบการเปลี่ยนแปลงการผูกมัดก่อน/หลังการรักษาหรือความเครียด
✓ ทําแผนที่เครื่องหมายฮิสโตนที่สัมพันธ์กับสถานะโครมาตินที่ใช้งานอยู่หรือถูกกดขี่
✓ สร้างหลักฐานสําหรับกลไกใน epigenetics, เนื้องอกวิทยา, ภูมิคุ้มกันวิทยา และการพัฒนา
เวิร์กโฟลว์หลักใน 6 ขั้นตอน
ผู้เริ่มต้นส่วนใหญ่ประสบความสําเร็จเร็วขึ้นเมื่อพวกเขาปฏิบัติต่อ ChIP เป็นห่วงโซ่ของขั้นตอนที่ "ต้องไม่หยุด" ไม่ใช่การทดลองเพียงครั้งเดียว นี่คือลําดับการปฏิบัติเบื้องหลัง ChIP: เปิดเผยว่าโปรตีนควบคุมยีนอย่างไร:
• แก้ไข (ไม่บังคับ แต่พบได้ทั่วไป): โปรโตคอล ChIP จํานวนมากใช้การเชื่อมขวางแบบย้อนกลับได้ ซึ่งมักจะใช้ฟอร์มาลดีไฮด์ 1% เป็นเวลา ~10 นาที จากนั้นจึงดับ (โดยทั่วไปจะใช้ไกลซีน)
• การเตรียมการสลาย/โครมาติน: กําหนดมาตรฐานผลผลิตนิวเคลียส/โครมาตินเพื่อความสม่ําเสมอ
• การตัดดีเอ็นเอ: การกระจายตัวควบคุมความละเอียดและอัตราการเพิ่มคุณค่า
• การตกตะกอนของภูมิคุ้มกัน: ความจําเพาะของแอนติบอดีเป็นตัวกําหนดหลักของ S/N
• การกลับตัวแบบ Cross-link (ถ้าใช้) และการทําให้บริสุทธิ์ DNA: ความบริสุทธิ์ที่สูงขึ้นจะเพิ่มความไวในการทดสอบ
• อ่านออก: ใช้ ChIP-qPCR สําหรับคําถามที่มุ่งเน้น หรือ ChIP-seq สําหรับการทําแผนที่ทั่วทั้งจีโนม
CTA เทคโนโลยี Longlight: หากคุณกําลังตั้งค่าเวิร์กโฟลว์ ChIP แรก โปรดติดต่อทีมของเราเพื่อขอรายการตรวจสอบตั้งแต่ต้นจนจบ (samp เป็นข้อมูล) ที่ตรงกับประเภทเป้าหมายของคุณ (TF เทียบกับเครื่องหมายฮิสโตน) และแผนการอ่านข้อมูลของคุณ (qPCR เทียบกับการจัดลําดับ)
การกระจายตัวและการเชื่อมโยงข้าม: การตั้งค่าสองอย่างที่ตัดสินผลลัพธ์ของคุณ
หากผลลัพธ์ ChIP ของคุณรู้สึก "สุ่ม" สาเหตุที่แท้จริงมักจะเป็นต้นน้ํา การตั้งค่าสองแบบมีอิทธิพลเหนือความสามารถในการทําซ้ํา:
ความแข็งแรงและเวลาในการเชื่อมขวาง การเชื่อมขวางอย่างหนักสามารถทําให้ปฏิสัมพันธ์ที่อ่อนแอมีเสถียรภาพ แต่ยังสามารถลดผลผลิต DNA และทําให้ขั้นตอนปลายน้ําซับซ้อนขึ้นอีกด้วย โปรโตคอลมาตรฐานหลายรายการอ้างถึงฟอร์มาลดีไฮด์ 1% ที่มีหน้าต่างการฟักตัวที่อุณหภูมิห้องสั้น เช่น ~10–15 นาที ตามด้วยการดับ
ขนาดชิ้นส่วน สําหรับการใช้งาน ChIP ส่วนใหญ่ ช่วงการตัดที่แนะนําโดยทั่วไปคือ ~200–600 bp ซึ่งสร้างสมดุลระหว่างความละเอียดกับความสามารถในการกู้คืนในเซลล์และเนื้อเยื่อ
✓ ขนาดใหญ่เกินไป (เช่น >800–1000 bp) มักจะลดความละเอียดและเพิ่มพื้นหลัง
✓ ขนาดเล็กเกินไปสามารถทําลาย epitopes ลด DNA ที่กู้คืนได้ หรือไลบรารีอคติ
✓ การตั้งค่า "ที่ดีที่สุด" ขึ้นอยู่กับเครื่องมือและตัวอย่าง ดังนั้นการเพิ่มประสิทธิภาพจึงเป็นเรื่องปกติ ไม่ใช่ความล้มเหลว
นี่คือความจริงที่ซ่อนอยู่เบื้องหลัง ChIP: เผยให้เห็นว่าโปรตีนควบคุมยีนอย่างไร: การวิเคราะห์ปลายน้ําที่สะอาดที่สุดไม่สามารถช่วยชีวิตการเตรียมโครมาตินที่ไม่สอดคล้องกันได้
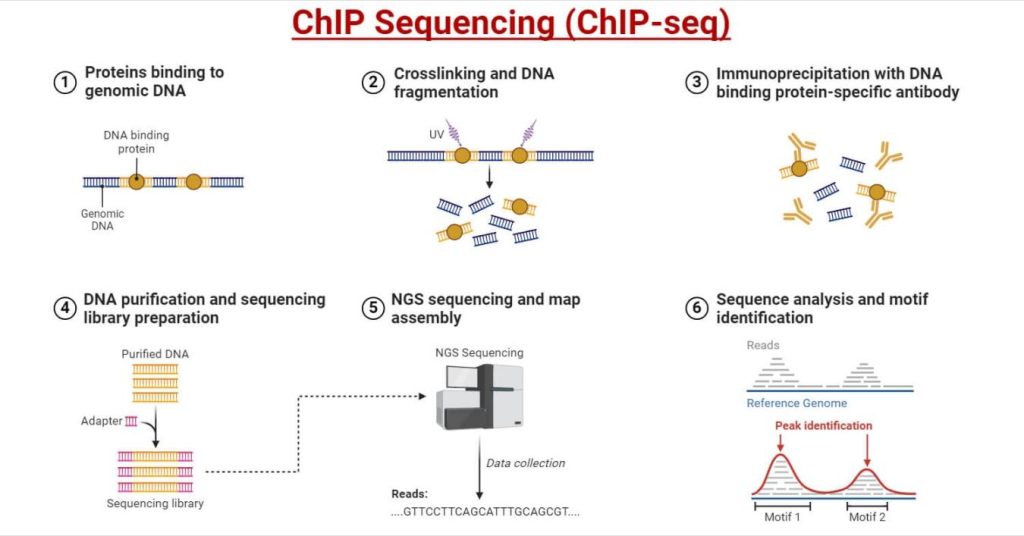
ChIP Sequencing (ChIP-seq): หลักการ ขั้นตอน การใช้งาน ไดอะแกรม
แอนติบอดี การควบคุม และ "การเพิ่มคุณค่าที่ดี" มีลักษณะอย่างไร
ChIP เป็นการทดสอบที่ขับเคลื่อนด้วยแอนติบอดี ดังนั้นแอนติบอดีเป้าหมายและการควบคุมของคุณจะกําหนดว่าข้อมูลของคุณจะเชื่อถือได้หรือไม่
การควบคุมที่คุณควรวางแผนตั้งแต่วันแรก:
✓ป้อน DNA (เศษเสี้ยวของโครมาตินก่อน IP) เพื่อทําให้การฟื้นตัวเป็นปกติ
✓การควบคุม IgG เพื่อวัดพื้นหลังแบบดึงลงที่ไม่เฉพาะเจาะจง
✓ ตําแหน่งบวกที่ทราบ (ถ้ามี) เพื่อยืนยันว่าระบบทํางานอยู่
ความคาดหวังในการเพิ่มความสมบูรณ์ตามความเป็นจริงจะแตกต่างกันไปตามประเภทเป้าหมาย ตัวอย่างเช่น ผู้ให้บริการบางรายรายงานว่าการเพิ่มคุณค่าของปัจจัยการถอดความ/ปัจจัยร่วม ChIP อาจต่ําถึง ~0.5% ของอินพุตทั้งหมด ในขณะที่ ChIP การดัดแปลงฮิสโตนอาจสูงขึ้นอย่างมาก (หลายสิบเปอร์เซ็นต์) ขึ้นอยู่กับความอุดมสมบูรณ์ของเครื่องหมายและประสิทธิภาพของแอนติบอดี พื้นหลัง IgG ทั่วไปพร้อมลูกปัดสามารถอยู่ที่ประมาณ ~0.05–0.1% ของอินพุต
ช่วงนั้นไม่ได้มีไว้เพื่อข่มขู่คุณ แต่มีไว้เพื่อปกป้องคุณจากความคาดหวังที่ผิดพลาด ใน ChIP: เผยให้เห็นว่าโปรตีนควบคุมยีนอย่างไร "เล็ก" ยังคงถูกต้อง ตราบใดที่มันมีความเฉพาะเจาะจง ทําซ้ําได้ และอยู่เหนือพื้นหลังด้วยการควบคุมที่เหมาะสม
CTA เทคโนโลยี Longlight: หากคุณกําลังแก้ไขปัญหาพื้นหลังสูงหรือสัญญาณอ่อน ให้ขอเทมเพลตการออกแบบการควบคุมจากเรา (กลยุทธ์ไพรเมอร์ การวางแผนเศษส่วนอินพุต และเกณฑ์พื้นหลัง) เพื่อให้คุณสามารถวินิจฉัยคอขวดได้อย่างรวดเร็ว
ChIP-qPCR Vs ChIP-seq: การเลือกการอ่านค่าที่เหมาะสมสําหรับเป้าหมายของคุณ
กฎที่เป็นมิตรกับผู้เริ่มต้นคือ: qPCR ตอบว่า "มีไหม" ในขณะที่เรียงลําดับคําตอบว่า "อยู่ที่ไหนอีก"
ChIP-qPCR เหมาะอย่างยิ่งเมื่อคุณมีพื้นที่ที่น่าสงสัยชุดเล็กๆ (โปรโมเตอร์/ตัวเพิ่มประสิทธิภาพ) และคุณต้องการการทําซ้ําอย่างรวดเร็ว นอกจากนี้ยังเป็นก้าวสําคัญในทางปฏิบัติก่อนลงทุนในการจัดลําดับ
ChIP-seq เป็นตัวเลือกสําหรับการค้นพบและการทําแผนที่ทั่วทั้งจีโนม แต่ต้องมีการวางแผนสําหรับตัวชี้วัดความลึกและคุณภาพ คําแนะนํา ENCODE ให้เป้าหมายที่อ้างอิงโดยทั่วไป เช่น
สําหรับปัจจัยการถอดความ / การทดลองสูงสุดแคบ: ชิ้นส่วนที่ใช้งานได้ขั้นต่ํา ~10 ล้านชิ้นต่อการทําซ้ํา โดยมีเป้าหมายที่แนะนําสูงกว่า
สําหรับเครื่องหมายฮิสโตนแบบกว้าง: ชิ้นส่วนที่ใช้งานได้ขั้นต่ํา ~20 ล้านชิ้นต่อการทําซ้ํา โดยมีเป้าหมายที่แนะนําสูงกว่าโดยขึ้นอยู่กับเป้าหมาย
ตัวเลขเหล่านี้ไม่ใช่แค่ "คําแนะนําในการจัดลําดับ" พวกเขากําหนดปริมาณวัสดุเริ่มต้นที่คุณต้องการแอนติบอดีของคุณต้องเข้มงวดเพียงใดและคุณต้องจัดการผลกระทบแบบแบทช์อย่างระมัดระวังเพียงใด นั่นคือเหตุผลที่ ChIP: Revealing How Proteins Control Genes มักชนะหรือแพ้ในขั้นตอนการออกแบบ
Qubit Assay Tubes และข้อได้เปรียบของบริการ ChIP-Seq: หนึ่งเวิร์กโฟลว์หนึ่งมาตรฐาน
จากตัวอย่างสู่รายงาน
เพื่อให้ ChIP: การเปิดเผยว่าโปรตีนควบคุมยีนอย่างไรเป็นประโยชน์สําหรับไทม์ไลน์การวิจัยจริงเวิร์กโฟลว์จะต้องสอดคล้องกันตั้งแต่การบริโภคตัวอย่างไปจนถึงการตีความขั้นสุดท้าย Longlight Technology จับคู่วัสดุสิ้นเปลืองที่เชื่อถือได้ เช่น Qubit Assay Tubes กับบริการ ChIP-seq แบบ end-to-end ที่ออกแบบมาเพื่อลดการส่งต่อ ควบคุมความแปรปรวน และทําให้ผลลัพธ์ง่ายต่อการตีความสําหรับผู้เริ่มต้นและทีมที่มีประสบการณ์
บริการแบบครบวงจรที่ขจัดปัญหาคอขวด
รูปแบบการบริการของเราออกแบบมาสําหรับห้องปฏิบัติการที่ต้องการผลลัพธ์ ChIP-seq โดยไม่ต้องสร้างไปป์ไลน์การจัดลําดับเต็มรูปแบบภายในองค์กร คุณจัดเตรียมตัวอย่างเซลล์คงที่หรือตัวอย่างเนื้อเยื่อแช่แข็ง และเราทําตามขั้นตอนที่เหลือด้วยจุดตรวจที่ได้มาตรฐาน:
✓ การเตรียมตัวอย่างและการยอมรับ QC
✓ การควบคุมการตัดและการกระจายตัวของโครมาติน
✓ การก่อสร้างห้องสมุดและห้องสมุด QC
✓ การจัดลําดับบนเครื่องมือและ QC ข้อมูล
✓ การวิเคราะห์ชีวสารสนเทศและการรายงานที่มีโครงสร้าง
✓ การส่งรายงานที่สมบูรณ์และข้อมูลดิบ
การตรวจสอบคุณภาพอย่างเข้มงวดในทุกลิงค์
ChIP-seq ขึ้นอยู่กับประสิทธิภาพสัญญาณต่อสัญญาณรบกวน ความแปรผันของกระบวนการที่ละเอียดอ่อนในการจัดการ การตัด หรือเมตริกไลบรารีสามารถเจือจางสัญญาณที่แท้จริงได้ เทคโนโลยี Longlight ใช้การควบคุม QC ที่เข้มงวดตลอดเพื่อให้สามารถเพิ่มคุณค่าได้อย่างมั่นใจและการตีความการผูกมัดที่ชัดเจน
✓ QC ทีละขั้นตอนเพื่อป้องกันความสามารถในการทําซ้ํา
✓ การตรวจสอบคุณภาพข้อมูลที่สอดคล้องกับ QC การทดลองกับการวิเคราะห์ปลายน้ํา
✓ การรายงานที่สะอาดซึ่งช่วยให้คุณค้นหาการผูกมัดที่ยีนหรือภูมิภาคเฉพาะด้วยความมั่นใจที่สูงขึ้น
เหมาะสําหรับตัวอย่างขนาดเล็ก
ทีมวิจัยจํานวนมากทํางานกับวัสดุที่จํากัด โดยเฉพาะอย่างยิ่งเมื่อศึกษาเซลล์ปฐมภูมิ เนื้อเยื่อหายาก หรือตัวอย่างในระยะเริ่มต้น ขั้นตอนการทดลองที่ปรับให้เหมาะสมของเราได้รับการออกแบบมาเพื่อทําการทดลองและวิเคราะห์ ChIP-seq ให้เสร็จสมบูรณ์แม้ว่าการป้อนตัวอย่างจะถูกจํากัดก็ตาม
✓ การเพิ่มประสิทธิภาพกระบวนการสําหรับโครงการที่มีอินพุตต่ํา
✓ คําแนะนําในการออกแบบที่ใช้งานได้จริงเพื่อหลีกเลี่ยง "ลูปการทํางานซ้ํา" ที่เกิดจาก QC ไม่เพียงพอ
✓ เวิร์กโฟลว์ที่เสถียรเพื่อช่วยให้การศึกษาตัวอย่างขนาดเล็กยังคงตีความได้
คําถามที่กําหนดเป้าหมาย: ยีนหรือภูมิภาคเฉพาะ หรือการค้นพบทั่วทั้งจีโนม
ChIP ศึกษาปฏิสัมพันธ์ระหว่างโปรตีนและดีเอ็นเอในลักษณะที่สะท้อนถึงบริบทของโครมาตินที่แท้จริง ChIP-seq รวม ChIP เข้ากับการจัดลําดับรุ่นต่อไปเพื่อตรวจจับไซต์ DNA ที่ผูกมัดโดยปัจจัยการถอดความเฉพาะหรือฮิสโตนทั่วทั้งจีโนม การวิเคราะห์ของเราสามารถสนับสนุนทั้งงานที่มุ่งเน้นและขับเคลื่อนด้วยการค้นพบ ทั้งนี้ขึ้นอยู่กับเป้าหมายของคุณ
ChIP-seq สามารถช่วยคุณตอบคําถามเช่น:
✓เปรียบเทียบตําแหน่งที่โปรตีนปรากฏในไซต์และแผนที่การผูกมัดในบริเวณจีโนมเป้าหมาย
✓สํารวจว่ารูปแบบการดัดแปลงฮิสโตนเกี่ยวข้องกับการเปลี่ยนแปลงการแสดงออกของยีนอย่างไร
✓ระบุตําแหน่งที่แม่นยําของ RNA polymerase II และไซต์จับทรานส์แฟกเตอร์อื่น ๆ
✓ ศึกษาปัจจัยการถอดความเพื่อเชื่อมโยงการผูกมัดกับผลลัพธ์ด้านกฎระเบียบ
ทําไมต้องเลือกเทคโนโลยี Longlight
Longlight Technology รองรับจีโนมสมัยใหม่ด้วยระบบนิเวศของผลิตภัณฑ์และบริการที่ใช้งานได้จริง นอกเหนือจากบริการ ChIP-seq แล้ว เรายังมีเครื่องมือที่เกี่ยวข้องกับ NGS เช่น Focused Ultrasonicator รวมถึงรีเอเจนต์และวัสดุสิ้นเปลืองคุณภาพสูงที่ใช้ในสถานศึกษา คลินิก และอุตสาหกรรม
✓ วัสดุสิ้นเปลืองและชุดอุปกรณ์: เจลอะกาโรสสําเร็จรูป, เครื่องกําจัดกรดนิวคลีอิก, หลอดคิวบิต, ชุดสกัดกรดนิวคลีอิก และชุดเตรียมห้องสมุด
✓ โซลูชั่นจีโนมิกส์: ผลิตภัณฑ์ที่ออกแบบมาเพื่อปรับปรุงประสิทธิภาพ ความแม่นยํา และความสามารถในการทําซ้ําในห้องปฏิบัติการ
✓ การสนับสนุนการวิจัย: คําแนะนําเวิร์กโฟลว์ที่ช่วยให้ทีมย้ายจากตัวอย่างไปสู่ข้อสรุปที่ใช้งานได้
ประเด็นสุดท้าย
ChIP: เปิดเผยว่ายีนควบคุมโปรตีนทํางานอย่างไร ได้ดีที่สุดเมื่อคุณปฏิบัติต่อยีนเป็นระบบควบคุม: การเตรียมโครมาตินที่เสถียร แอนติบอดีที่ผ่านการตรวจสอบแล้ว การควบคุมที่ซื่อสัตย์ และการอ่านข้อมูลที่ตรงกับคําถามของคุณ หากคุณสร้างเวิร์กโฟลว์ด้วยตรรกะนั้น ChIP จะกลายเป็นหนึ่งในหน้าต่างที่ชัดเจนที่สุดในการควบคุมยีนที่คุณสามารถใช้ในห้องปฏิบัติการสมัยใหม่ได้
หากคุณต้องการ ให้แบ่งปันประเภทเป้าหมายของคุณ (TF เทียบกับเครื่องหมายฮิสโตน) และรูปแบบตัวอย่าง (เซลล์เทียบกับเนื้อเยื่อ) และฉันสามารถร่างรายการตรวจสอบเวิร์กโฟลว์ที่เป็นมิตรกับผู้เริ่มต้นและจุด QC ที่เหมาะกับกรณีการใช้งานของคุณ โดยยังคงอยู่ในรูปแบบที่ชัดเจนและอ่านง่ายเหมือนเดิม